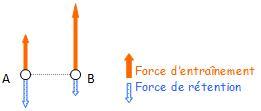
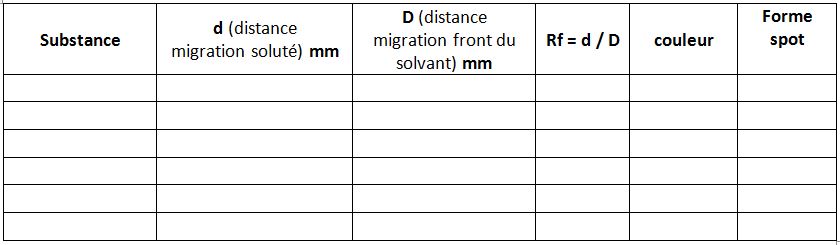
Lait : analyse qualitative des glucides par chromatographie sur couche mince
Date de dernière mise à jour : 06/03/2024
Commentaires
-
 Bonjour,
Bonjour,
Tout d'abord je vous remercie pour votre site qui est une source d'inspiration! Cependant je me permets de vous contacter pour vous poser une question concernant la défécation acide du lait. Comment procédez-vous? Avec de l'acide trichloroacétique ou avec de l'acide acétique?
Merci d'avance pour votre réponse. -
 Bonjour
Bonjour
je voudrai réaliser cette expérience avec mes eleves
mais je n'arrive pas à avoir une belle révélation de la CCM. Quel réactif de révélation utilisez vous ?
Merci par avance
cordialement Voici deux exemples de révélation : http://droguet-sebastien.e-monsite.com/pages/activites-technologiques-terminale-2014-2015/at06.html
Voici deux exemples de révélation : http://droguet-sebastien.e-monsite.com/pages/activites-technologiques-terminale-2014-2015/at06.html
- l'aniline donne de belles colorations mais les risques liés à l'utlisation de ce réactif (cf fiche toxicologique de l'INRS : http://www.inrs.fr/publications/bdd/fichetox/fiche.html?refINRS=FICHETOX_19 mènent à ne plus l'employer en prébac.
- une alternative consiste à substituer l'aniline par du permanganate ; c'est moins joli, mais les risques sont limités.
Il convient de mettre en oeuvre les neufs principes de prévention suivants, régis par l'article L4121-2 du code du travail : https://www.legifrance.gouv.fr/affichCodeArticle.do?idArticle=LEGIARTI000006903148&cidTexte=LEGITEXT000006072050
1° Eviter les risques ;
2° Evaluer les risques qui ne peuvent pas être évités ;
3° Combattre les risques à la source ;
4° Adapter le travail à l'homme, en particulier en ce qui concerne la conception des postes de travail ainsi que le choix des équipements de travail et des méthodes de travail et de production, en vue notamment de limiter le travail monotone et le travail cadencé et de réduire les effets de ceux-ci sur la santé ;
5° Tenir compte de l'état d'évolution de la technique ;
6° Remplacer ce qui est dangereux par ce qui n'est pas dangereux ou par ce qui est moins dangereux ;
7° Planifier la prévention en y intégrant, dans un ensemble cohérent, la technique, l'organisation du travail, les conditions de travail, les relations sociales et l'influence des facteurs ambiants, notamment les risques liés au harcèlement moral et au harcèlement sexuel, tels qu'ils sont définis aux articles L. 1152-1 et L. 1153-1, ainsi que ceux liés aux agissements sexistes définis à l'article L. 1142-2-1 ;
8° Prendre des mesures de protection collective en leur donnant la priorité sur les mesures de protection individuelle ;
9° Donner les instructions appropriées aux travailleurs.
Substituer l'aniline par le permanganate répond au principe n°6.
-
 Bonjour,
Bonjour,
Pour notre épreuve de TPE, avec mon groupe nous souhaiterions réaliser à la chromatographie de différents laits (nous travaillons sur l'intolérance au lactose ) mais nous n'arrivons pas à trouver le bon éluant, pouvez vous me dire ce que vous avez utilisé ?
Merci d'avance
Alice Durand Bonsoir,
Bonsoir,
Voici deux éluants qui sont des mélanges de solvant pour lesquels je vous invite à rechercher les fiches de sécurité (FDS) afin de vérifier si vous avez l'équipement nécessaire pour les utiliser :
• solvant glucide 1 :
méthyléthylcétone (butanone) 3 Volumes
acide éthanoïque 1 Volume
éthanol 1 Volume
• solvant glucide 2 :
n-butanoi 5 Volumes
isopropanol 3 Volumes
eau distillée 1 Volume
Le solvant 1 migre très rapidement (15 min) et la séparation est correcte
Le solvant 2 migre trois fois plus lentement
=> à tester, comparer en terme d'efficacité de séparation et choisir en fonction du temps disponible
Ajouter un commentaire